Di alam terdapat banyak senyawa dengan karakteristik masing-masing. Adanya kesamaan karakteristik menjadikan kita mudah untuk menggolongkan senyawa-senyawa yang ada.
Misalnya, senyawa organik dan senyawa anorganik. Setiap senyawa memiliki nama spesifik untuk membedakannya dari senyawa lain.
Penulisan namanya dapat dituliskan secara sistematik atau menurut IUPAC-International Union of Pure and Applied Chemistry), maupun ditulis berdasarkan nama lazim (nama dagang).
Pada kesempatan kali ini, kita akan membahas bagaimana cara penulisan tata nama dari senyawa-senyawa yang telah disebutkan di atas secara sistematik.
Tata Nama Senyawa Organik
Senyawa organik adalah senyawa kimia yang mengandung karbon yang memiliki sifat-sifat tertentu, kecuali karbida, karbonat, dan oksida karbon.
Dalam sistem penamaannya, senyawa organik relatif lebih kompleks dibandingkan dengan senyawa anorganik.
Tidak hanya berdasarkan rumus molekulnya, namun juga berdasarkan rumus struktur kimia dan gugus fungsinya.
Dalam bab ini, hanya akan dibahas cara penamaan senyawa organik yang sederhana.
| Gugus Fungsi*) | Rumus Senyawa | Rumus Struktur*) | Nama IUPAC |
| Alkana | CH4 | 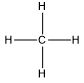 | Metana |
| Keton / Alkanon | C3H6O | 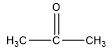 | 2-propanon |
| Alkena | C5H10 | 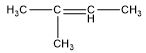 | 2-metil-2-pentena |
| Alkohol / Alkanol | C4H9OH | 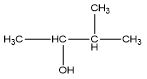 | 3-metil-2-butanol |
| Aldehida / Alkanal | CH2O | | Metanal |
| dll. |
*) Masih banyak lagi
Baca juga Koloid.
Tata Nama Senyawa Anorganik
Senyawa anorganik adalah senyawa kimia yang tidak mengandung karbon. Senyawa anorganik dikelompokkan menjadi senyawa ion, senyawa molekul, dan asam.
1. Senyawa Ion
Senyawa ion terdiri dari kation (unsur logam) dan anion (unsur non logam atau poliatom). Senyawa ion dapat berupa senyawa basa maupun garam. Rumus senyawa ion ditentukan oleh perbandingan muatan kation dan anionnya.
Rumus : Ax+ + By+ → AyBx
Cara penulisan nama senyawa ion :
- Nama kation di depan dan nama anion di belakang, angka indeks tidak ditulis.
- Kation diberi nama sama dengan unsur logamnya. Jika logam memiliki bilangan oksidasi (biloks) beragam, maka biloks logam ditulis dengan angka romawi dalam tanda kurung.
- Anion monoatom atau poliatom tanpa unsur oksigen diberi nama akhiran “-ida”. Anion poliatom yang mengandung unsur oksigen diberi nama akhiran “-at” atau “-it” sesuai banyaknya jumlah atom O, kecuali pada anion OH–.
Berikut ini beberapa jenis kation dan anion.
| Rumus Kation | Nama Kation | Rumus Anion | Nama Anion |
| Na+ | Natrium | OH– | Hidroksida |
| Mg2+ | Magnesium | Cl– | Klorida |
| Fe2+ | Besi(II) | NO3– | Nitrat |
| Cu+ | Tembaga(I) | SO42- | Sulfat |
| NH4+ | Amonium | CrO42- | Kromat |
Contoh :
- NaOH = natrium hidroksda
- KNO3 = kalium nitrat
- FeCl2 = besi(II) klorida
- K2CrO4 = kalium kromat
2. Senyawa Molekul
Senyawa molekul terdiri dari unsur-unsur non logam. Pada bab ini hanya akan dibahas cara penamaan dari senyawa molekul biner (senyawa molekul yang mengandung dua jenis unsur).
Ada 2 cara penulisan nama senyawa molekul, yaitu :
Cara 1
- Unsur yang terletak lebih kiri pada sistem periodik unsur ditulis di depan. Kecuali pada senyawa yang mengandung oksigen dan halogen (kecuali fluorin), maka oksigen ditulis di belakang. Jika unsur-unsurnya terletak dalam satu golongan, maka yang letaknya lebih bawah ditulis di depan.
- Menentukan biloks unsur yang berada di depan lalu nilai biloks ditulis dengan angka romawi dalam tanda kurung. Unsur yang berada di belakang diberi nama akhiran “-ida”.
Contoh :
- N2O5 = nitrogen(IV) oksida
- SO3 = sulfur(VI) oksida
Cara 2
- Unsur yang terletak lebih kiri pada sistem periodik unsur ditulis di depan. Kecuali pada senyawa yang mengandung oksigen dan halogen (kecuali fluorin), maka oksigen ditulis di belakang. Jika unsur-unsurnya terletak dalam satu golongan, maka yang letaknya lebih bawah ditulis di depan.
- Menyebutkan jumlah unsur dengan bahasa latin (mono, di, tri, tetra, dst.). Namun jika unsur yang berada di depan hanya 1, tidak perlu ditulis “mono-“. Unsur yang berada di belakang diberi nama akhiran “-ida”.
Contoh :
- N2O5 = dinitrogen pentaoksida
- SO3 = sulfur trioksida
3. Asam
Asam adalah senyawa yang mengandung ion H+ dan anion. Cara penulisannya adalah dengan menulis kata “asam” dan diikuti nama anion.
Contoh :
- HCl = asam klorida
- HF = asam fluorida
- H3PO4 = asam fosfat
Baca juga Reaksi Kimia.
Contoh Soal Tata Nama Senyawa
1. Secara sistematik, tuliskan nama dari senyawa-senyawa berikut.
- a. Ca3(PO)4
- b. Fe(NO3)2
- c. K2Cr2O7
- d. H2SO4
- e. N2O3
a. Ca3(PO)4 = kalsium fosfat
Karena terdiri dari kation Ca2+ dan anion PO43-, maka termasuk dalam senyawa ion.
b. Fe(NO3)2 = besi(II) nitrat
Karena terdiri dari kation Fe2+ dan anion NO3–, maka termasuk dalam senyawa ion.
c. K2Cr2O7 = kalium dikromat
Karena terdiri dari kation K+ dan anion Cr2O72-, maka termasuk dalam senyawa ion.
d. H2SO4 = asam sulfat
Karena mengandung ion H+ dan anion SO42-, maka termasuk dalam asam.
e. N2O3 = nitrogen(III) oksida = dinitrogen trioksida
Karena terdiri dari unsur-unsur non logam, maka termasuk dalam senyawa molekul.
2. Tuliskan rumus kimia dari nama-nama senyawa berikut.
- a. Difosfor pentaoksida
- b. Sulfur(IV) oksida
- c. Kalsium klorat
- d. Timah(IV) klorida
- e. Asam karbonat
- a. P2O5 (senyawa molekul)
- b. SO2 (senyawa molekul)
- c. Ca(ClO3) (senyawa ion)
- d. SnCl4 (senyawa ion)
- e. H2CO3 (asam)
Demikian pembahasan mengenai tata nama senyawa. Semoga dapat bermanfaat. Baca juga Perkembangan Teori Atom.
